
Critérios para análise de relevância e aplicabilidade dos estudos incluídos
Para que seja elaborada uma avaliaçăo clínica, é preciso haver fundamentaçăo em resultados de investigaçőes clínicas prévias do próprio dispositivo a ser registrado ou compilaçăo da literatura científica existente de dispositivos equivalentes. Com relaçăo ŕ segunda forma, como classificar e selecionar os estudos ideais para a criaçăo de um relatório de avaliaçăo clínica de boa qualidade?
Durante as buscas iniciais nas bases de dados, săo encontrados estudos de diversos delineamentos. Nesta fase muitos já săo excluídos por năo se tratarem de estudos com alto nível de evidęncia. Os critérios de exclusăo geralmente envolvem estudos que contenham apenas resumo, artigos em animais, análises in vitro, revisőes (sem resultados clínicos) e protocolos de ensaios clínicos (descrevem apenas os detalhes de como o estudo foi conduzido).
De acordo com o guia MEDDEV e o guia 31 (ANVISA) para avaliaçőes clínicas de dispositivos médicos, o delineamento experimental ideal para inclusăo na avaliaçăo clínica săo ensaios clínicos que reúnam as características de um estudo pivotal. Estudos de metodologia pivotal utilizam grupo comparador ativo, com objetivo de demonstrar năo inferioridade ou superioridade, contemplando desfecho primário que tenha natureza clínica e com tempo de follow-up que seja capaz de identificar tanto eventos agudos quanto tardios.
Os ensaios clínicos randomizados cumprem este critério, sendo amplamente reconhecidos como referęncia para obtençăo de resultados de segurança e eficácia, objetivo principal do relatório de avaliaçăo clínica. Além deste delineamento, estudos observacionais, como coortes prospectivas ou retrospectivas, com longo período de acompanhamento dos pacientes também podem ser utilizados. Estes estudos apresentam a vantagem de avaliar possíveis desfechos que podem năo ocorrer em curto prazo, mas aparecem alguns anos após o uso do dispositivo.
Após a criteriosa seleçăo dos estudos a serem incluídos no relatório, o próximo passo se trata da análise de relevância e aplicabilidade. Essa avaliaçăo é importante pois a incerteza pode surgir de duas fontes: a qualidade metodológica e a relevância dos dados para a avaliaçăo do dispositivo em relaçăo aos diferentes aspectos de sua finalidade pretendida. Ambas as fontes de incerteza devem ser analisadas para determinar uma ponderaçăo para cada conjunto de dados.
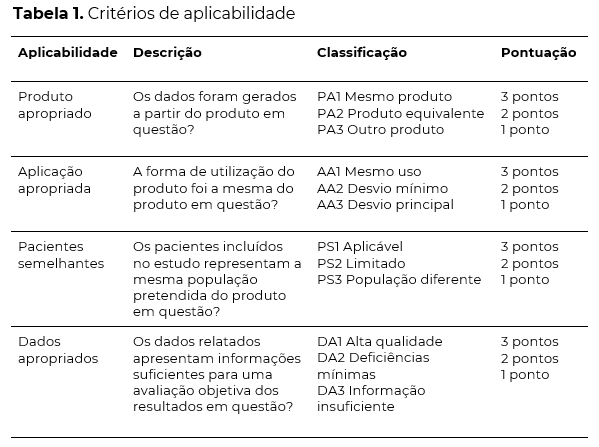
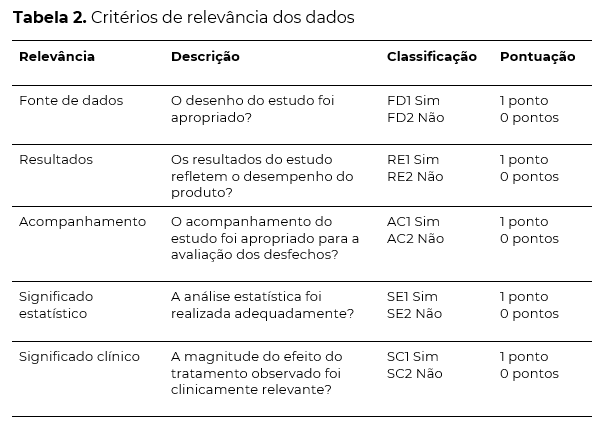
Portanto, para a avaliaçăo de aplicabilidade várias características dos artigos săo analisadas, incluindo pacientes semelhantes, produto, aplicaçăo e dados apropriados. Somado a isso, os estudos também săo classificados em relevância clínica, de acordo com sua fonte de dados, seus resultados, acompanhamento, significado estatístico e clínico.
Estas escalas, apresentadas nas tabelas 1 e 2, podem variar de 1 a 3 pontos para cada critério de aplicabilidade ou de 0 a 1 ponto para os índices de relevância. Cada estudo recebe uma pontuaçăo conforme sua qualidade em cada critério mencionado acima. A pontuaçăo máxima que cada artigo pode receber é de 17 pontos. Para ser considerado na análise, o estudo deve apresentar um mínimo de 14 pontos, correspondendo a 80% dos pontos possíveis. Caso o estudo năo atinja a pontuaçăo mínima, é desconsiderado da avaliaçăo clínica.
A existęncia de todas essas análises de qualidade dos estudos tanto nas buscas primárias quanto nesta avaliaçăo secundária permitem concluir que apenas estudos de alta evidęncia científica sejam incluídos no relatório final. Para a obtençăo do registro por meio da avaliaçăo clínica é imprescindível que sejam selecionados estudos pivotais ou artigos de outros delineamentos que obtenham pontuaçăo adequada nos critérios de relevância e aplicabilidade.
Referęncias
- MEDDEV 2.7/1. revision 4. CLINICAL EVALUATION: A GUIDE FOR MANUFACTURERS AND NOTIFIED BODIES UNDER DIRECTIVES 93/42/EEC and 90/385/EEC. Disponível em: https://ec.europa.eu/docsroom/documents/17522/attachments/1/translations/en/renditions/native
- ANVISA. Guia de Avaliaçăo Clínica de Dispositivos Médicos. Guia no 31/2020, versăo 2. Disponível em: http://www.so.com.br/legislacao_anvisa/2020/Guia%20Anvisa%20-%20Avalia%C3%A7%C3%A3o%20Cl%C3%ADnica%20de%20Dispositivos%20M%C3%A9dicos%20-%2023-07-2020.pdf